
地址 : 江苏省苏州市吴江区汾湖高新技术产业开发区金字路8号
邮编 : 215001
电话 :0512-80673999
E-mail : 401916004qq.com
电话 :(086)512-6693 6472
手机 :189 1409 1973
传真 :(086)512-6752 9886
E-mail :3250139710@qq.com

核准日期:2021年10月19日
修改日期:
头孢地尼颗粒说明书
请仔细阅读说明书并在医师指导下使用
【药品名称】
通用名称:头孢地尼颗粒
英文名称:Cefdinir Granules
汉语拼音:Toubaodini Keli
【成份】
本品主要成份为头孢地尼。
化学名称:(6R,7R)-7-[[(2-氨基-4-噻唑基)-(肟基)乙酰基]氨基]-3-乙烯基-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-羧酸
化学结构式:
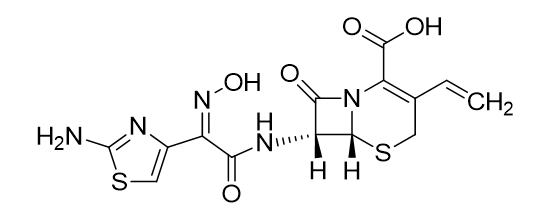
分子式:C14H13N5O5S2
分子量:395.42
【性状】
本品为混悬颗粒,气芳香,味甜。
【适应症】
对头孢地尼敏感的葡萄球菌属、链球菌属、肺炎球菌、大肠杆菌、克雷白氏菌、奇异变形杆菌、流感嗜血杆菌等菌株所引起的下列感染:毛囊炎、疖、疖肿、痈、传染性脓痂疹、丹毒、蜂窝组织炎、淋巴管炎、炭疽、化脓性甲沟炎、皮下脓肿、汗腺炎、粉瘤感染、慢性脓皮症。咽喉炎、急性支气管炎、扁桃腺炎症、肺炎。肾盂肾炎、膀胱炎。猩红热。中耳炎、副鼻窦炎。
【规格】
50mg
【用法用量】
成人服用的常规剂量为一次2袋(100mg效价),一日3次。儿童服用的常规剂量为每日9~18mg(效价)/kg,分3次口服。可依年龄、症状进行适量增减。
【不良反应】
在使用本品治疗的13,715名患者中,有354例(2.58%)不良反应(包括实验室数据异常)的报告。主要不良反应为消化道症状(110例,0.80%),如腹泻或腹痛;皮肤症状(31例,0.23%),如皮疹或瘙痒。主要的实验室数据异常包括谷丙转氨酶(126例,0.92%)和谷草转氨酶(89例,0.65%)升高;嗜酸性粒细胞增多(41例,0.30%)。
(1)严重的不良反应
1)休克:偶有休克发生(发生率低于0.1%),要严密观察。当有不适感、口内异常感、喘鸣、眩晕、便意、耳鸣、出汗等症状时应立即停药并进行适当处理。
2)过敏反应:可能会出现过敏(呼吸困难、红斑、血管性水肿、荨麻疹等)(低于0.1%),需要严密观察,出现异常症状应立即停药并进行适当处理。
3)皮肤科:可能发生史-约综合征(低于0.1%)或毒性表皮坏死松解症(低于0.1%)。应严密观察患者,若出现发热、头痛、关节痛、皮肤或粘膜出现红斑/水泡、皮肤感觉紧绷/灼烧/疼痛,应立即停药并进行适当处理。
4)血液学:可能发生全血细胞减少症(低于0.1%)、粒细胞缺乏症(低于0.1%,初期症状为发热、咽喉痛、头痛、不适)、血小板减少症(低于0.1%,初期症状为瘀斑、紫癜)或溶血性贫血(低于0.1%,初期症状为发热、血红蛋白尿、贫血症状)。应定期严密观察患者,若出现异常情况,应立即停药并进行适当处理。
5)结肠炎:可能发生严重的结肠炎(低于0.1%),如经血便证实的伪膜性结肠炎。应严密观察患者,如果患者出现腹痛或频繁腹泻等症状,应立即停药并进行适当处理。
6)间质性肺炎或PIE综合征:可能发生经发热、咳嗽、呼吸困难、胸部X光检查异常或嗜酸粒细胞增多证实的间质性肺炎或PIE综合征(都低于0.1%)。若出现此类症状,应立即停药并进行适当处理,如使用肾上腺皮质激素类药物。
7)肾脏疾病:可能发生严重肾脏疾病(低于0.1%),如急性肾衰竭。应定期严密观察患者,若出现异常情况,应立即停药并进行适当处理。
8)暴发性肝炎、肝功能异常或黄疸:可能发生严重肝炎(低于0.1%),如伴有明显谷丙转氨酶、谷草转氨酶或碱性磷酸酶升高的暴发性肝炎、肝功能异常(低于0.1%)或黄疸(低于0.1%)。应定期严密观察患者,若出现异常情况,应立即停药并进行适当处理。
(2)其他不良反应
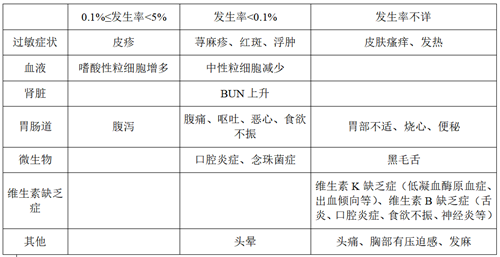
注)若出现异常情况,应立即停药并进行适当处理。
【禁忌】
对本品有休克史者禁用。对青霉素或头孢菌素有过敏史者慎用。
【注意事项】
1.谨慎使用(下列患者应慎用)
(1)对青霉素类抗生素有过敏史者。
(2)本人或亲属中有易发生支气管哮喘、皮疹、荨麻疹等过敏症状体质者。
(3)严重的肾功能障碍者:由于头孢地尼在严重肾功能障碍患者血清中存在时间较长,应根据肾功能障碍的严重程度酌减剂量以及延长给药间隔时间。对于进行血液透析的患者,建议剂量一日1次,一次100mg。
(4)患有严重基础疾病、不能很好进食或非经口摄取营养患者、全身状况恶劣的患者(因可能会出现维生素K缺乏,要进行严密临床观察)。
(5)原则上应在确认微生物对头孢地尼的敏感性后使用本剂,限于治疗患者所需的最短周期内防止耐药菌的产生。
(6)建议避免与铁剂合用。如果合用不能避免,应在服用本剂3小时以后再使用铁剂。
2.重要的基本注意事项
因有出现休克等过敏反应的可能,应详细询问过敏史。
3.对临床检验值的影响
(1)除试纸法尿糖试验之外,在用Benedict试剂、Fehling试剂和Clinitest试验法进行尿糖检查时,可出现假阳性,要注意。
(2)可出现直接血清抗球蛋白试验阳性,要注意。
4.其它注意事项
(1)与添加铁的产品(如奶粉或肠营养剂)合用时,可能出现红色粪便。
(2)可能出现红色尿。
【孕妇及哺乳期妇女用药】
有关妊娠期的用药,其安全性尚未确立。对孕妇或怀疑有妊娠的妇女,用药要权衡利弊,只有在利大于弊的情况下,才能使用。尚不知本品是否在乳汁中有分布,哺乳期妇女用药要权衡利弊,只有在利大于弊的情况下,才能使用。
【儿童用药】
对于体重过低的早产儿、新生儿的用药安全性尚未确立。(使用经验较少)
【老年用药】
老年患者使用本品时应特别注意以下方面,并根据对患者的临床观察调整剂量和给药间隔:
1、由于身体机能下降,老年患者可能容易出现不良反应。
2、由于维生素K缺乏,老年患者可能会有出血倾向。
【药物相互作用】
本品与下列药物合用时需慎重。
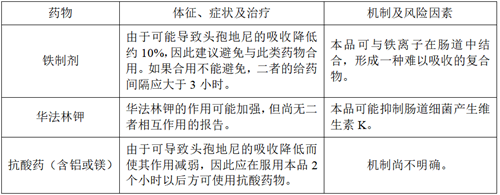
【药物过量】
超剂量使用头孢地尼没有进行研究。在急性、毒性、侵蚀性溃疡的研究中,单一口服5600mg/kg剂量并未产生不良反应。而其他β-内酰胺类抗性素,超剂量用药时可表现出以下不良反应:恶心、呕吐、腹泻和惊厥。血清透析可以清除人体内的头孢地尼。对超剂量用药引起毒性反应的患者,血清透析是有效的,尤其是肾功能不全患者。
【药理毒理】
药理作用
作用机制
同其他头孢类抗菌药物,头孢地尼通过抑制细菌细胞壁的合成而起杀菌作用。头孢地尼对部分β-内酰胺酶稳定,因此,许多青霉素和头孢菌素类耐药的细菌对头孢地尼敏感。
耐药机制
头孢地尼的耐药机制主要为:β-内酰胺酶的水解、青霉素结合蛋白(PBPs)改变和膜通透性降低。头孢地尼对大多数肠杆菌属、假单胞菌、肠球菌、耐青霉素链球菌和耐甲氧西林葡萄球菌无活性。β-内酰胺酶阴性的耐氨苄青霉素流感嗜血杆菌对头孢地尼不敏感。
抗菌活性
体外及临床感染中,头孢地尼对下列微生物的大多数菌株有抗菌活性(见【适应症】)。
革兰阳性菌
金黄色葡萄球菌(仅限甲氧西林易感菌株)
肺炎链球菌(仅限青霉素易感菌株)
化脓性链球菌
革兰阴性菌
流感嗜血杆菌
副流感嗜血杆菌
卡他莫拉菌
以下体外试验数据可用,但其临床意义未明。头孢地尼对至少90%的下列微生物的体外最低抑菌浓度(MIC)小于或等于1μg/ml。然而,尚未在充分且良好对照的临床试验中获得头孢地尼治疗这些微生物所致的临床感染的有效性数据。
革兰阳性菌
表皮葡萄球菌(仅限甲氧西林易感菌株)
无乳链球菌
草绿色链球菌
革兰阴性菌
柯氏柠檬酸杆菌
大肠埃希菌
肺炎克雷伯菌
变形杆菌
敏感性试验方法
在可能的情况下,临床微生物实验室应定期向医生报告并提供其所在医院所使用的抗菌药物的相关体外药敏性试验结果,该结果可反映医院及社区获得性病原菌的药敏特点。这些报告可帮助医生在治疗时选择抗菌药物。
稀释法
采用定量方法测定最小抑菌浓度(MIC),这些最小抑菌浓度值可用于评估细菌对抗菌药物的敏感程度。应采用标准测试方法(肉汤法或琼脂法)来测定MIC,可根据表1中的标准对测定的MIC值进行解释。
扩散法
采用对抑菌圈直径进行测定的定量方法,同样可对细菌对抗菌药物的敏感性进行可重复性估计。抑菌圈的大小代表着细菌对抗菌药物敏感程度,应采用标准测试方法进行测定。该法使用浸渍着5μg的头孢地尼的纸片对细菌对抗菌药物的敏感程度进行测定,纸片扩散情况依据表1中的标准进行判定。
表1.头孢地尼敏感性试验判定标准
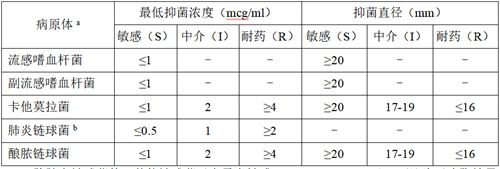
a除肺炎链球菌外,其他链球菌对青霉素敏感(MIC≤0.12μg/ml),可认为对头孢地尼敏感。
b肺炎链球菌对青霉素敏感(MIC≤0.06μg/ml),可认为对头孢地尼敏感。肺炎链球菌分离株的敏感性试验检测1μg苯唑西林的抑菌直径≥20mm即为对青霉素敏感,可认为对头孢地尼敏感。不推荐对青霉素中介和耐药的分离株进行头孢地尼敏感性测试,未获得可靠的头孢地尼敏感性试验判定标准。
葡萄球菌对头孢地尼的敏感性可通过测试青霉素和头孢西丁或甲氧西林来推断。对甲氧西林或头孢西丁敏感的葡萄球菌可认为对头孢地尼敏感。
药敏报告“敏感”表示,如果当抗菌药物在感染部位达到有效浓度,病原菌很大程度上会被抑制生长。报告“中介”表示,该结果是不明确的,如果微生物对可替换的临床可行药物不完全敏感,则应重复进行该测试。这个分类意味着在药物生理性聚集的身体部位或在能使用高剂量的情况下可能的临床适用性。这个分类还能提供一个缓冲空间来防止小的、不受控制的技术因素导致的解释差异。报告“耐药”表示,如果抗菌药物在感染部位能达到有效浓度而很大程度不能抑制病原体的生长的,则应该采取其他的治疗方法。
质量控制
标准化药敏试验过程要求利用实验室监控并确保测定过程中供试品和分析试剂的准确度和精密度,以及个人操作实验的技术水平。应提供具有表2中MIC值的头孢地尼粉末标准品。对于使用扩散法的5μg的头孢地尼纸片的抑菌直径标准应该符合表2的数值。
表2.头孢地尼可接受的质量控制范围
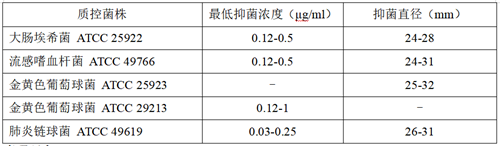
毒理研究
遗传毒性
头孢地尼在Ames试验和中国仓鼠V79细胞HGPRT点突变试验中结果均为阴性;在体外中国仓鼠V79细胞染色体畸变试验和小鼠骨髓细胞微核试验中试验结果均为阴性。
生殖毒性
大鼠经口给予头孢地尼1000mg/kg/天(以mg/kg/天计为70倍人用剂量;以mg/m2/天计为11倍人用剂量)未见对生育力和生殖行为有损害。
妊娠大鼠经口给予头孢地尼1000mg/kg/天(以mg/kg/天计为70倍人用剂量;以mg/m2/天计为11倍人用剂量),妊娠兔经口给予头孢地尼10mg/kg/天(以mg/kg/天计为0.7倍人用剂量;以mg/m2/天计为0.23倍人用剂量)未见致畸作用。10mg/kg/天组妊娠兔可见母体毒性(体重降低),对胎仔未见影响。在围产期毒性试验中,≥100mg/kg/天组仔鼠体重降低,≥32mg/kg/天组大鼠子代体重降低。但母体生殖参数和子代生存率、发育、行为和生殖功能均无异常。
【药代动力学】
1、吸收
– 6名健康成人一次空腹口服50、100、200mg(效价)头孢地尼时,约经4小时后可达到血药峰浓度,分别为0.64、1.11和1.74μg/ml,其血浆半衰期为1.6~1.8小时。
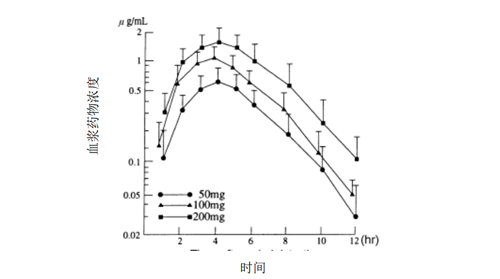
男性健康成人单次口服头孢地尼后的血浆药物浓度曲线
– 6名健康成人一次空腹和进食后口服100mg(效价)头孢地尼,约经4小时后,可达到血药峰浓度,分别为1.25、0.79μg/ml。进食后给药,其吸收稍有降低。
– 肾功能受损患者一次口服100mg(效价)头孢地尼,血浆半衰期随肾功能下降而延长。
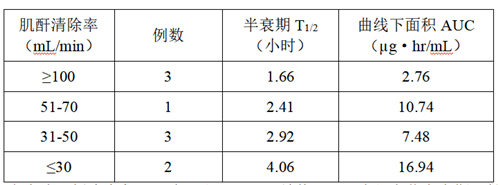
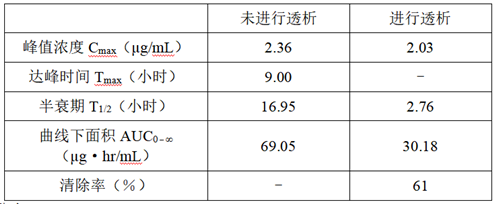
– 6名血液透析患者餐后一次口服100mg(效价)后,本品血浆半衰期延长近11倍。在相同的患者中餐后一次口服100mg(效价)头孢地尼,在血药浓度达峰值时血液透析4小时。进行血液透析者的半衰期缩短,约为不进行血液透析者的1/6,清除率为61%。
2、分布
在患者痰液、扁桃体、上颌窦粘膜组织、中耳分泌物、皮肤组织和口腔组织等均有分布,尚不知是否在乳汁中有分布。
3、代谢
人体血液、尿及粪便中未发现有抗菌活性的代谢产物。
4、排泄
头孢地尼主要经肾脏排泄。
– 健康成人(空腹)口服50、100、200mg(效价)时,尿排泄率(0~24小时)约为26~33%,4~6小时的尿液峰值浓度分别为44.3、81.5和132μg/ml。
– 肾功能受损患者一次口服100mg(效价)头孢地尼,排泄缓慢,并与肾受损程度成正比。
【贮藏】 遮光,密封,室温保存。
【包装】 聚酯/铝/聚乙烯药品包装用复合膜包装,6袋/盒,8袋/盒,9袋/盒,10袋/盒,12袋/盒,16袋/盒。
【有效期】 24个月
【执行标准】 YBH13022021
【批准文号】 国药准字H20213789
【药品上市许可持有人及生产企业】
药品上市许可持有人及企业名称:苏州第三制药厂有限责任公司
药品上市许可持有人及生产地址:苏州市吴江区汾湖高新技术产业开发区金字路8号
邮政编码:215211
联系方式:0512-80673990
传 真:0512-80673998